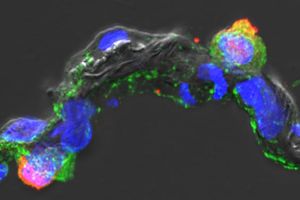
Das Bild zeigt die ausgedehnte Infektion von menschlichen Lungenbläschen durch MERS-CoV (grün) im direkten Vergleich zum hochpathogenen Influenzavirus H5N1 (rot). Bei der Studie wurde das Lungengewebe gleichzeitig mit beiden Viren infiziert. Während H5N1-Influenzaviren nur eine Zellart der Lungenbläschen ("Typ II Zellen") befallen, infiziert das MERS-CoV alle Zellen, womit das Lungenversagen bei schwer erkrankten Patienten erklärt werden könnte.
Das neuartige MERS-Coronavirus (MERS-CoV) führt zu einer massiven Infektion des menschlichen Lungengewebes, die in ihrem Ausmaß weit über eine Infektion mit dem gefährlichen H5N1-Influenzavirus hinausgeht. Das konnte nun ein deutsches Wissenschaftlerteam der Charité - Universitätsmedizin Berlin und des Robert-Koch-Institutes in explantiertem menschlichen Lungengewebe herausfinden.
Der Einsatz einer speziellen mikroskopischen Technik ermöglicht eine Darstellung der Infektion, des Rezeptors für die Viren und des verursachten Schadens in der Lunge.
Seit 2012 erkrankten vor allem in Ländern der arabischen Halbinsel über 130 Menschen an dem neuartigen MERS-CoV (Middle East Respiratory Syndrome Coronavirus). Über 50 Patienten verstarben an der Infektion. Das Virus löst eine schwere Infektion der Lunge aus. Über die Krankheitsmechanismen im Menschen liegen bislang nur sehr eingeschränkte Informationen vor.
Eiweiß als Eintrittspforte für Viren vermutet
Das Forscherteam nutzte explantiertes menschliches Lungengewebe, um Mechanismen der Infektion zu untersuchen. Im direkten Vergleich mit hochpathogenen H5N1-Influenzaviren stellte sich heraus, dass sich beide Viren nahezu gleich stark im Gewebe vermehren können. Während sich das Influenzavirus jedoch in nur einem Zelltyp vermehrt, infiziert das Coronavirus nahezu alle Zelltypen der Lungenbläschen. "Wir waren von der ausgedehnten Infektion im Vergleich zu den hochpathogenen Influenzaviren völlig überrascht", sagt Stefan Hippenstiel von der Berliner Charité.
Die Mikroskopie von menschlichem Lungengewebe wird normalerweise von dessen starker Eigenfluoreszenz behindert. "Durch den Einsatz einer speziellen mikroskopischen Technik gelang es uns jedoch, dieses Hemmnis zu überwinden. So konnten wir nun auf subzellulärer Ebene die Lungenschäden beschreiben", erklärt Andreas Hocke, der ebenfalls an der Studie mitwirkte.
Außerdem konnten die Forschern auch den Eiweißstoff DPP4 in allen befallenen Zelltypen nachweisen. Die Experten vermuten deshalb, dass die Viren DPP4 als Eintrittspforte in die menschlichen Zellen nutzen. (red, derStandard.at, 2.10.2013)