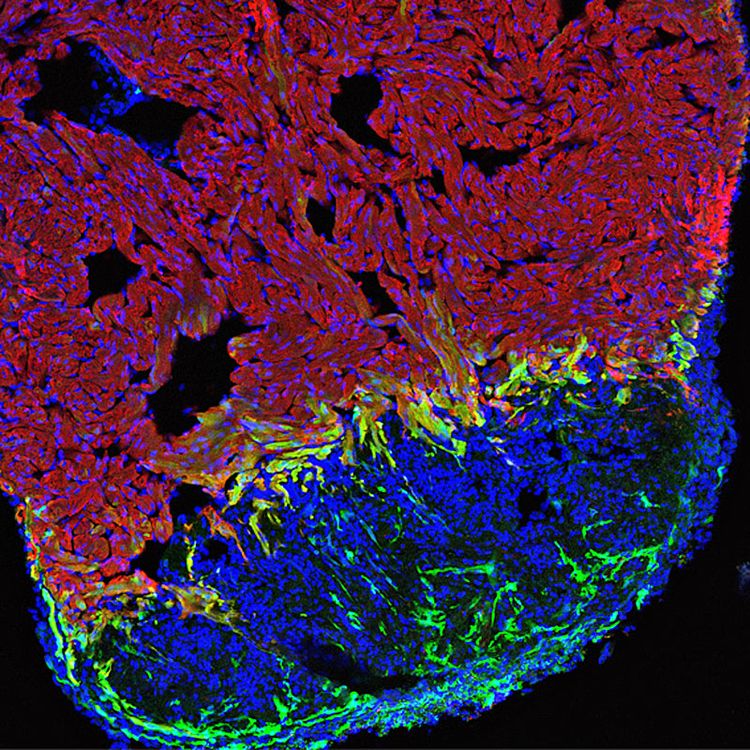
Für diese mikroskopische Aufnahme eines Gewebeschnittes durch ein regenerierendes Herz wurde das gesunde Muskelgewebe rot, die Wunde blau und aktivierte Herzmuskelzellen grün gefärbt.
Ulm – Zebrafische (eigentlich Zebrabärblinge) werden in der Genetik und Entwicklungsbiologie häufig als Modellorganismen verwendet. Einer der Gründer dafür liegt in ihrer bemerkenswerten Regenerationsfähigkeit: Die Fische können wichtige Organe und verletzte Extremitäten nachwachsen lassen. Sogar Verletzungen am Herzen heilen bei Zebrafischen wieder vollständig aus. Nun haben Forscher der Universitäten Utrecht und Ulm einen zentralen molekularen Mechanismus entschlüsselt, über den dieser Heilungsprozess gesteuert wird.
"Das verletzte Gewebe regeneriert sich durch die vermehrte Zellteilung von Herzmuskelzellen an der Wundgrenze", erklärt Gilbert Weidinger von der Universität Ulm. Gemeinsam mit Kollegen berichtet er im Fachblatt "Developmental Cell" nun, wird die Zellvermehrung über ein besonderes Protein gesteuert wird: das sogenannte bone morphogenetic protein (BMP).
Aktivitätsatlas
BMP ist ein wichtiges Signalprotein der Zell-Zell-Kommunikation. Die Forscher konnten nachweisen, dass es insbesondere im Wundbereich re-aktiviert wird, wo gesundes und verletztes Gewebe aufeinander treffen. Dafür haben die Molekularbiologen ein spezielles Verfahren zur Sequenzierung von RNA entwickelt, über das es möglich ist, im Wundbereich und den benachbarten Gewebsregionen die Aktivität diverser Gene genau zu lokalisieren.
"So entsteht ein genomweiter Atlas an regional sehr unterschiedlichen Expressions- und Aktivitätsmustern, die im regenerierenden Herzen Aufschluss darüber geben, welche Gene und Zell-Signale im gesunden und im verletzten Gewebe, beziehungsweise genau an der Wundgrenze aktiviert sind", so Erstautor Chi-Chung Wu.
Auf diese Weise wurde ersichtlich, dass das BMP-Signal von Herzmuskelzellen aktiviert wird, die aus dem Grenzbereich zwischen gesundem und verletztem Herzmuskelgewebe kommen. Mit Hilfe von transgenen Zebrafischlinien, bei denen der BMP-Signal-Weg einerseits blockiert und andererseits verstärkt wurde, konnten die Forscher den Regenerationsprozess gezielt beeinflussen. Bei der genetisch veränderten Variante mit blockiertem BMP-Signal-Weg waren Zellvermehrung und damit die Regenerationsfähigkeit deutlich reduziert. Bei der Variante mit überaktivem BMP konnte die Regeneration dagegen sogar forciert werden.
Therapiepotenzial
"Das BMP-Signal ist auch in verletzten Maus-Herzen aktiv, aber dort reagieren die Herzzellen völlig anders darauf: sie sterben. Hier wird durch BMP also keine Regeneration ausgelöst, sondern die beschädigten Zellen werden stattdessen in den `Selbstmord´ getrieben", sagt Koautor Jeroen Bakkers vom Universitätsklinikum Utrecht.
Die Wissenschaftler wollen nun herausfinden, wieso Herzzellen in Zebrafischen und in Säugetieren so unterschiedlich reagieren und welche Prozesse letztendlich dafür verantwortlich sind. "Vielleicht wird es eines Tages möglich sein, die Regenerationsfähigkeit von menschlichem Herzgewebe durch entsprechende Medikamente oder Therapien, die auf der Grundlage solcher Forschungsergebnisse entwickelt wurden, deutlich zu verbessern", hoffen die Forscher. (red, 6. 2. 2016)