
Sie ist nicht nur extrem genau, sondern auch günstig: Die Technologie, die als "Genschere" Crispr/Cas9 bekannt wurde, ist heute aus der Forschung nicht mehr wegzudenken. Zwei Forscherinnen, die maßgeblich an ihrer Entwicklung beteiligt waren, erhielten 2020 dafür den Chemienobelpreis, Emmanuelle Charpentier und Jennifer Doudna. Anwendung hat sie in den vergangenen Jahren vor allem auch bei der Pflanzenzucht gefunden: Crispr sorgt für viel geringere und gezieltere Veränderungen als die traditionellen Zuchtmethoden aus dem 20. Jahrhundert, die etwa auf radioaktive Bestrahlung und dadurch verursachte zufällige Genmutationen setzten.
Nun sind Behörden einen wichtigen Schritt bei den medizinischen Anwendungen gegangen. Gentherapien mit anderen Methoden gibt es bereits mehrere, doch erstmals wurde eine auf Crispr basierende Gentherapie zugelassen: In Großbritannien gab kürzlich die Arzneimittelbehörde MHRA grünes Licht für eine Anwendung namens Exa-cel, die dort den Handelsnamen Casgevy trägt. Zwei Bluterkrankungen können damit therapiert werden: Sichelzellanämie und Beta-Thalassämie.
Die Gen-Schere CRISPR/Cas-9 ermöglicht es, genetische Veränderungen so schnell und so kostengünstig wie nie zuvor durchzuführen. Die Methode hat das Zeug dazu, die Welt, wie wir sie kennen, zu verwandeln. Der Bericht zum Video auf: https://derstandard.at/2000097747118/Wie-die-Genschere-CRISPR-unsere-Welt-veraendern-kann
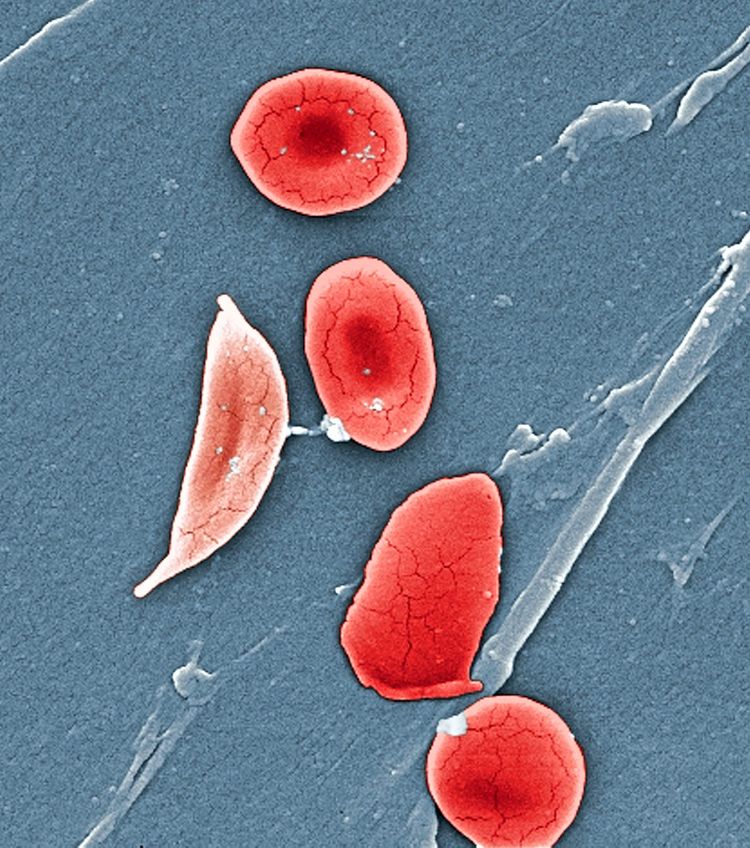
Beide Erbkrankheiten gehen meist mit schwerwiegenden, schmerzhaften Symptomen einher und können zum Tod führen. Bei der Sichelzellanämie sind die roten Blutkörperchen länglich verformt. Sie können starr werden und wesentlich schlechter Sauerstoff transportieren. Betroffen sind vor allem Menschen vom afrikanischen Kontinent, dem Mittelmeerraum und solche, die Vorfahren aus diesen Regionen haben. Die sichelförmigen Zellen könnten einigen Betroffenen sogar einen Vorteil gegenüber der Infektionskrankheit Malaria bieten, doch zu einem hohen Preis. Wird sie nicht früh diagnostiziert, sterben Patientinnen und Patienten meist an den Folgen der Sichelzellanämie, die etwa zu verstopften Gefäßen, Organschäden, starken Schmerzen und verschlimmerten Infektionen führt.
Auch die seltenere Beta-Thalassämie ist insbesondere im Mittelmeerraum verbreitet. Erkrankte haben ebenfalls einen Gendefekt, der den Blutfarbstoff Hämoglobin betrifft: Dieser Komplex, der im Blut Sauerstoff transportiert, wird nicht ausreichend funktionsfähig gebaut. Patientinnen und Patienten sind von Medikamenten und Bluttransfusionen alle zwei bis vier Wochen abhängig.
Blut wie ein kleines Baby
In Österreich dürften statistisch mehrere Hundert Personen von den Blutkrankheiten betroffen sein, die vergleichsweise häufig vorkommen, sagt Selim Corbacioglu vom Universitätsklinikum Regensburg: "Darum sind diese Leiden für die Pharmahersteller natürlich von Interesse." An seiner Klinik sei im Zuge der Zulassungsstudie weltweit der erste Patient mit dieser Crispr-basierten Gentherapie behandelt worden.
Diese Therapie ist komplizierter als ein einzunehmendes Medikament: Von Betroffenen müssen Blutstammzellen gewonnen werden, in denen durch die Genschere stillgelegte Gene wieder aktiviert werden. Durch diesen Trick soll der Körper eine Hämoglobinform herstellen, die er einst im ungeborenen Stadium und in den ersten Lebensmonaten produzierte und die mehr Sauerstoff transportieren kann. Dafür kommen die modifizierten Stammzellen nach einer Chemotherapie ähnlich wie bei einer Blutwäsche zurück in die Blutbahn der Patientin oder des Patienten. Vereinfacht ausgedrückt klingen die Symptome also stark ab, weil man Blut produziert wie ein junges Baby.
Chemotherapien haben starke Nebenwirkungen und sind bei anderen Heilungsversuchen der Bluterkrankungen nötig. So können bereits Stammzellen von gesunden Menschen transplantiert werden. "Der große Vorteil der Crispr-Therapie ist, dass es anders als bei der Stammzelltransplantation weder eine Immunreaktion des Körpers (die zu einer Abstoßung führt) noch eine Immunreaktion des Spenders gibt", sagt Corbacioglu. "Denn es sind ja die eigenen Zellen, die zurück in den Körper kommen."
Die Ergebnisse der klinischen Studien sind vielversprechend: Der Großteil der Probandinnen und Probanden mit Beta-Thalassämie benötigte am Ende des Studienzeitraums keine Bluttransfusionen mehr, Patientinnen und Patienten mit Sichelzellanämie hatten keine Schmerzkrisen mehr, sagt Corbacioglu.
Aufwendiges Verfahren
Gleichzeitig sei zu beachten, dass bei den Zulassungsstudien nur wenige Personen getestet wurden und das bis maximal vier Jahre nach dem Eingriff. "Nebenwirkungen sind weiterhin denkbar", sagt der Facharzt. Es könne prinzipiell sein, dass die Beschwerden zurückkehren. Zu 100 Prozent könne nicht ausgeschlossen werden, dass in den Zellen andere DNA-Abschnitte als die anvisierten verändert werden. Durch die Chemotherapie werden Betroffene unfruchtbar, in seltenen Fällen können sie dadurch an Krebs erkranken. Weiterhin müssen Behandelte beobachtet werden.
Es wird allerdings nicht die DNA in den Keimzellen verändert. Das bedeutet: Wenn beispielsweise einer Patientin vor der Therapie entnommene Eizellen befruchtet eingesetzt werden und sie schwanger wird, könnte sie die Erbkrankheit an Nachkommen weitergeben. Ein weiteres Problem skizziert Joachim Kunz vom Universitätsklinikum Heidelberg, ebenfalls ein Experte auf diesem Gebiet, der zudem mehrere Firmen berät: "Werden Frauen nach der Gentherapie schwanger, kann die Sauerstoffversorgung des ungeborenen Kindes vermindert sein, weil das mütterliche Hämoglobin den Sauerstoff nicht leicht genug abgibt."
Während Crispr viel rascher, einfacher und genauer anzuwenden ist als vergleichbare Methoden, ist die Bearbeitung der Stammzellen für Patientinnen und Patienten dennoch relativ aufwendig. Aufgrund der benötigten Ressourcen wird die Prozedur jährlich nur einer begrenzten Patientenzahl zur Verfügung stehen, sagt Kunz.
Zulassung in der EU
Erschwerend kommt der hohe Preis hinzu: Pro Person soll die Crispr-Gentherapie 1,5 bis 2 Millionen Euro kosten. Im Vergleich dazu ist die bisherige Stammzelltransplantation mit maximal 300.000 Euro günstiger, sagt Corbacioglu. Sie birgt aber auch höhere Risiken und steht nur etwa 20 Prozent der Sichelzellerkrankten zur Verfügung, da nur etwa für diese Zahl geeignete Stammzellspender und -spenderinnen gefunden werden, betont Kunz. Die neuere Therapieform dürfte die ältere also eher ergänzen als ablösen. In Deutschland kämen von etwa 3.000 bis 4.000 Sichelzellkranken aus Altersgründen 500 bis 1.000 für die Crispr-Therapie infrage.
Auch in anderen Ländern könnte die neue Gentherapie bald eine Zulassung erhalten: In den USA wird darüber in den kommenden Wochen und Monaten entschieden, das Bewertungsverfahren der europäischen Arzneimittelagentur EMA ist noch im Gange.
Wird die Therapie erlaubt, muss dies aber nicht automatisch bedeuten, dass sie angeboten wird. Dies muss auch von Krankenkassen ausverhandelt werden, sagt Kunz. Und er nennt das Beispiel einer bereits existierenden Gentherapie bei Beta-Thalassämie, die 2022 in Deutschland auf den Markt kam und nicht auf Crispr basiert, aber ähnlich funktioniert. Innerhalb eines Jahres wurden neun Personen dadurch geheilt. "Allerdings hat sich das Unternehmen, das diese Therapie angeboten hat, vom deutschen Markt zurückgezogen, weil in den Verhandlungen mit den Kostenträgern nicht der erwünschte Preis erzielt werden konnte." (Julia Sica, 17.11.2023)